癌性爆发痛专家共识(2019年版)

中国抗癌协会癌症康复与姑息治疗专业委员会难治性癌痛学组 中华医学会疼痛学分会癌痛学组
关键词
癌性爆发痛 共识 阿片类药物 药物治疗
疼痛是恶性肿瘤患者最常见的症状之一,约80%肿瘤患者在其疾病诊疗过程中会出现癌性疼痛(简称癌痛)[1]。在癌痛患者中,癌性爆发痛(breakthrough cancer pain,BTcP)的发生率可达33%~95%,BTcP的存在,不仅严重影响患者的日常活动,导致生存质量、治疗依从性的下降,还会增加医疗资源的支出[2],而且常常提示临床预后较差且对阿片类药物治疗的抗拒[3]。BTcP为一种难治性癌痛,主要体现在疼痛多不可预测,病理机制复杂,任何解救性药物均有滞后性。虽然去除病因对于BTcP的治疗较为重要,但由于多数患者已处于肿瘤终末期,因而对抗肿瘤治疗的应答和耐受能力均下降。近年来,随着“癌痛规范化治疗示范病房”、“难治性疼痛示范基地”等项目的推广,国内对BTcP的关注日趋重视,但关于BTcP的诊断、评估、药物及非药物治疗等方面仍不规范。为此,由中国抗癌协会癌症康复与姑息治疗专业委员会难治性癌痛学组和中华医学会疼痛学分会癌痛学组牵头,组织国内相关领域专家经过多次研讨,借鉴国外相关指南、共识,并结合国内临床实践及治疗经验,编写完成《癌性爆发痛专家共识(2019年版)》,旨在为国内BTcP的诊疗提供依据。
1. 癌性爆发痛的定义和诊断标准
1.1 癌性爆发痛的定义
1990年,Portenoy等[4]首先提出BTcP的定义,是指在阿片类药物治疗疼痛稳定基础上出现的短暂性疼痛加重。在不同国家和地区,BTcP的定义和特征也不尽相同[5-6]。虽然国际上对BTcP的定义仍存争论,但普遍推荐2009年英国和爱尔兰姑息治疗协会(APM)[7]的定义,是指在背景痛控制相对稳定、镇痛药物充分应用的前提下,自发或在某些可预知或不可预知因素的诱发下突然出现的短暂疼痛加重。
1.2 癌性爆发痛的诊断标准
参照APM的诊断标准并紧密结合临床实践,本共识提出BTcP的诊断标准如下:
1)在过去的1周患者是否存在持续性疼痛(背景痛);
2)在过去的1周患者的背景痛是否充分控制(数字化疼痛评分≤3分);
3)患者是否存在短暂疼痛加重的现象(数字化疼痛评分≥4分)。
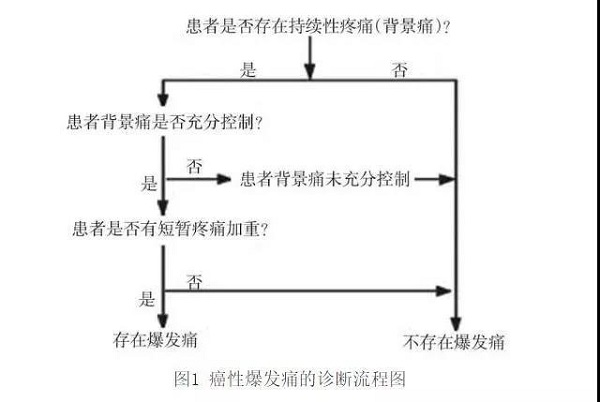
若上述问题的答案均为“是”,则可确诊患者存在BTcP。即上述3个条件需全部符合后,患者才可确诊存在BTcP。诊断流程详见图1。
2. 癌性爆发痛的分类
BTcP存在个体差异,在不同个体之间甚至同一个体内均具有可变性。BTcP存在不同的病理生理学特征(伤害感受性疼痛、神经病理性疼痛以及混合性疼痛),且可能与多种因素(肿瘤和肿瘤治疗相关以及其他良性疾病)有关。
BTcP通常分为两种亚型:
1)事件性BTcP(也称诱发性BTcP):一般是由可预测的因素所引起。
2)自发性BTcP(也称特发性BTcP):指在无任何特定活动或诱因的情况下发生的疼痛,具有不可预测性。
除上述外,还存在剂量末期疼痛(end-of-dose pain)[8],指由于镇痛药物剂量不足导致临近下次用药时,镇痛药物的血药浓度降低(低于镇痛最低浓度)而导致的疼痛。由于剂量末期疼痛具有可预测性,并且是由于药物按时作用且持续时间不足导致,可以通过调整定时给药的剂量或间隔时间获得缓解。因此,本共识推荐剂量末期疼痛不宜认为是BTcP的一个亚型。
3. 癌性爆发痛的评估
BTcP能否成功治疗取决于准确的评估、个体化的诊治和治疗后的再评估。遗憾的是,目前暂无公认且全面恰当的BTcP评估量表。根据2005年美国疼痛学会指南以及欧洲姑息治疗学会的推荐,全面的BTcP评估至少应包括发作频率、持续时间、疼痛强度、诱发缓解因素、与背景痛的关系以及背景痛的治疗效果。目前,国内最常用的评估工具主要为一维评估,包括数字化疼痛评分(numeric rating scales,NRS)、视觉模拟评分(visual analogue scales,VAS)和语言评分(verbal rating scales,VRS)。但一维疼痛评估量表并不能获得疼痛性质、伴随症状、部位以及对生存质量影响等相关信息。在国外较为常用的多维评估量表主要包括爆发痛问卷(breakthrough pain questionnaire,BPQ)和爆发痛评估工具(breakthrough pain assessment tool,BAT)。BPQ通过患者自我监测,对爆发痛的时间特征、严重程度、部位、病理生理机制、病因、诱发及缓解因素,以及与止痛药物的关系进行评估,具有全面及有针对性的特点,已广泛应用于BTcP的流行病学研究和药物研究。
BAT包括关于BTcP的时间、性质、强度等14项问题,每项均通过“0~10分”或“是与否”等形式进行具体量化,进一步简化了BTcP的评估,旨在促进BTcP患者的诊断、管理和定期监测。
4. 癌性爆发痛治疗原则
BTcP的治疗中,病因的治疗至关重要。如放疗可减轻癌性骨转移痛以及因肿瘤压迫导致的神经病理性疼痛等;化疗、内分泌治疗可减轻肿瘤对组织、内脏、神经的损伤或压迫;对于合并肠道梗阻的患者,可采用姑息手术治疗等。对于中晚期肿瘤,抗肿瘤治疗不能有效控制肿瘤时,病因治疗则显得极为困难,需要及时给予对症治疗。目前,国内外关于BTcP的治疗报道均是基于阿片类药物为主导的解救治疗,患者往往在出现疼痛后再给予解救药物。因此,疼痛的缓解具有滞后性。另外,解救药物的起效速度和安全性也是研究的重要内容,但即便是起效最快的制剂,也不能即刻有效缓解疼痛的突发性加重。国内仍以传统的即释吗啡作为主要的解救药物。而即释吗啡存在起效时间与爆发痛特征不相符的问题:相对快速起效的阿片类镇痛制剂,即释吗啡的起效时间为30~60 min,达到起效时,爆发痛可能已经自行缓解,镇痛效果有限,若增加阿片类药物会增加不良反应发生。鉴于此,在国内暂无快速起效BTcP解救药物的现状下,推荐患者自控镇痛(patient-controlled analgesia,PCA)的技术至关重要,一方面可以给予患者有效的BTcP解救,同时也可以给予及时的背景药物滴定。患者可根据疼痛的程度及时给药,可及时有效的控制爆发痛。治疗BTcP的PCA技术,一般采用静脉或皮下途径给药,临床常用的药物包括吗啡和氢吗啡酮注射剂。采用PCA技术不仅起效迅速、疗效安全,而且可有效地节省医疗资源。
通过研究国外文献和BTcP指南[7,9-13],专家组讨论提出,虽然国内暂无快速起效治疗BTcP的阿片类药物,但对于国外研究和临床应用的进展需有明确的认识,对在国际上有明确研究结果、临床已广泛应用且多项爆发痛专家共识均推荐的芬太尼制剂给予描述。由于BTcP具有不同特征,所以疼痛管理可能会涉及多种药物。除阿片类药物外,辅助镇痛药物,如抗抑郁药物、抗惊厥药物、非甾体类消炎药(nonsteroidal antiinflammatory drugs,NSAIDS)和对乙酰氨基酚,以及糖皮质激素等也可能对治疗BTcP有效,尤其对于阿片类药物反应差的疼痛控制至关重要。BTcP除解救药物治疗外,还应考虑局部靶点治疗方法。如骨转移导致的事件性BTcP,可以采用骨成形术、局部神经松解术和粒子植入术等,以及药物的联合应用,联合抗惊厥药物可以减少BTcP的次数。合理治疗方法的选择涉及BTcP的全面评估、明确BTcP的病理机制等方面。
5. 癌性爆发痛的药物治疗
5.1 阿片类止痛药物
5.1.1 肠内给药途径
1)口服给药途径:治疗BTcP的基本方法是使用解救药物。根据爆发痛的特点,理想的解救药物特点有起效迅速、作用持续时间短、耐受性好、不良反应小、使用方便、患者愿意使用、容易获得、费用低廉。临床上暂无能满足上述所有要求的解救药物。目前,限于国内暂无经黏膜芬太尼制剂,临床上多数采用即释阿片药物作为BTcP的解救药物。从药效学和药代动力学角度分析,经典的阿片药物口服即释吗啡片并非为治疗BTcP的最佳选择。但是对于发作缓慢、持续时间较长的BTcP,口服即释吗啡片仍为最常用的药物。目前,尚无证据支持BTcP的合理治疗剂量,大部分权威机构[14]建议使用每日背景阿片类镇痛剂量的10%~20%用于BTcP。欧洲姑息护理协会工作组建议使用每日背景阿片类镇痛剂的1/6。同时,又指出可能通过滴定才能确定治疗BTcP的最佳剂量。基于上述,本共识推荐应用每日背景剂量的10%~20%用于BTcP的初始剂量,同时根据止痛效果和不良反应逐步滴定。阿片类药物治疗BTcP的效果还取决于BTcP的发病特点,对于自发性BTcP,因为其不可预测,口服治疗往往不能及时起效。对于事件性BTcP,因为疼痛往往可以预测,可以在疼痛事件发生前给予口服速效阿片类药物,以预防和减轻事件性BTcP。因此,建议提前口服即释吗啡片,时间≥30 min(起效时间),或60 min(最大止痛效果)。口服即释吗啡片是预防和减轻事件性BTcP可选择的方法之一。对于吞咽片剂困难的患者,硫酸吗啡口服溶液可以作为替代药物。
2)直肠给药途径:直肠给药与口服给药相比吸收更快。此外,栓剂经过直肠黏膜静脉吸收后,部分药物直接进入体循环,不经过肝脏首过代谢。因此,可能比口服药物具有更高的生物利用度。但是,受直肠局部环境或药物放置位置的影响,直肠给药的生物利用度不稳定,且某些直肠疾患的患者不耐受或难以合作。因此,临床接受程度有限,不推荐作为常规的给药途径,可试用于部分口服困难的BPcP患者。
5.1.2 肠外给药途径
1)经黏膜途径:近年来研制的新型快速起效阿片类药物(rapid-onset opioids,ROOs)是专门用于治疗BTcP的镇痛药。ROOs均是基于芬太尼的制剂,经口腔或鼻腔黏膜给药,起效迅速、镇痛效能强、作用时间短,符合BTcP的发作特征。临床研究[15]表明,芬太尼经黏膜制剂治疗BTcP在起效时间和镇痛效果方面均优于安慰剂和传统的口服即释阿片类药物,推荐作为阿片类药物耐受患者快速发生BTcP的解救药物,或口服即释阿片药物解救无效的二线选择,但对于出现口腔、鼻腔黏膜损伤(如鼻咽癌放疗后损伤)的患者需要谨慎使用。
目前,国外[16]有多种ROOs用于临床,详见表1。
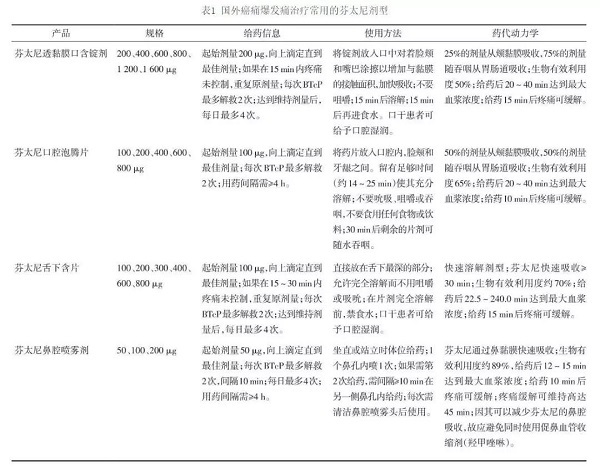
ROOs药物治疗BTcP需要滴定达到有效镇痛剂量。推荐ROOs治疗BTcP时需个体化滴定[17-18],对于应用较少阿片类药物的老年或身体比较虚弱的患者,需从最低剂量起始,逐渐向上滴定[19]。ROOs药物用于阿片类药物耐受患者BTcP的解救,可能会出现与阿片类药物相关的不良反应,如恶心、呕吐、头晕、嗜睡等,多发生在滴定阶段,程度通常轻到中度;ROOs药物反复应用可能出现给药途径相关的不良反应,如黏膜炎症、溃疡等,用药期间需密切观察。
2)其他途径:除黏膜给药以外,阿片类药物还可以通过其他途径使用。静脉途径因为起效迅速(5 min)和100%的生物利用度,在BTcP的使用中效果更为确切,通常仅限于住院的剧烈疼痛患者,并在患者疼痛改善后改为其他给药方式。皮下注射和肌肉内注射也是临床上较为常用的给药途径,其生物利用度较高(80%~100%),起效迅速(10~15 min)。吗啡肌肉内注射会增加局部刺激,长期反复应用存在吸收不稳定的风险,不推荐作为常规使用途径。PCA静脉及皮下给药也是临床上符合BTcP治疗的模式,经过简单的培训,各级医疗机构和护理人员均可应用该技术。对于口服药物困难,合并严重恶心、呕吐及消化道功能障碍的患者尤为适用。
5.2 非阿片类止痛药物
对于使用阿片类药物疗效欠佳的BTcP,除了考虑阿片类药物转换以外,还可根据疼痛机制应用辅助药物预防或减少BTcP。癌痛往往是复合性疼痛,依照世界卫生组织(WHO)的镇痛原则,对于单纯阿片药物控制欠佳的患者,推荐联合使用非阿片类镇痛药以及抗惊厥、抗抑郁等辅助药物。联合用药可减少单用阿片类药物疗效欠佳患者BTcP的发作次数,降低阿片类药物剂量,减少不良反应发生。与神经相关的BTcP可以通过联合抗惊厥、抗抑郁等辅助药物改善镇痛效果。对于脑转移或脑膜转移引起的颅内高压及脊髓压迫症状等相关性BTcP,可考虑应用脱水药物联合糖皮质激素治疗。对骨转移的癌症患者,在活动后会迅速出现疼痛,疼痛与骨破坏相关,此类患者可以考虑联合使用非甾体类抗炎药和双膦酸盐类药物。腹腔内脏器官痉挛而发生的BTcP可以考虑应用解痉药物治疗。
6. 癌性爆发痛的微创介入治疗
BTcP的微创介入治疗缺乏循证医学证据,多为难治性癌痛治疗的相关研究。从临床角度分析,由于BTcP大多与背景痛的病因相同,癌痛微创介入治疗即可有效控制疼痛,又可减少BTcP的发生。
微创介入治疗是通过下述几个途径达到减少BTcP及疼痛程度:1)减少肿瘤对组织、脏器、神经的损伤(如粒子植入术、瘤体物理或化学毁损);2)作用于神经传导通路,减少伤害性冲动向中枢神经系统的传导(如肋间神经损毁术、腹腔神经丛损毁术);3)改善组织结构和功能,提升组织结构的稳定性,减少事件性BTcP的发生(如经皮椎体成形术);4)通过改变给药途径或方式,提升镇痛药物治疗效果或加快起效时间(如PCA、鞘内药物输注系统)。鉴于BTcP的微创介入治疗与难治性癌痛相关,推荐参考《难治性癌痛专家共识》[20]相关内容。
7. 阿片类药物用于癌性爆发痛解救药物的风险评估及管理
阿片类药物规范用于癌痛患者,一般不会出现滥用和成瘾的问题,但考虑到BTcP的解救药物为短效、强效和高脂溶性阿片类药物,且常常需要多次使用。因此,本共识建议接受短效阿片类药物用于BTcP解救的患者应接受包括药品转移和阿片类药物相关异常行为[21](表2)的风险评估,针对高危患者给予个体化管理,并加强患者和家属的健康宣教。
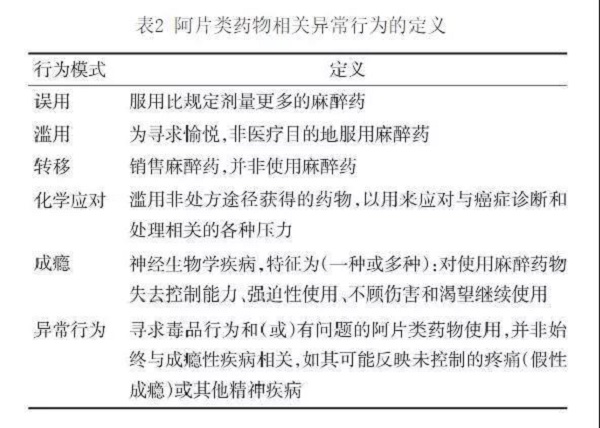
7.1 加强阿片类药物不恰当应用的风险评估
使用预测性好、可靠度高的评估工具。根据美国国立综合癌症网络(NCCN)成人癌痛指南[14]推荐,在服用阿片类药物前应用癌痛患者筛查及阿片类药物应用评估(screener and opioid assessment for patients with pain-revised,SOAPP-R)和阿片类药物风险评估工具(opioid risk tool,ORT)进行评估,在使用药物过程中可应用阿片类药物误用情况评估表(current opioid misuse measure,COMM)实时监测评估。
7.2 加强患者及其家属宣教工作
让患者及其家属认识到阿片类药物治疗的获益性及潜在风险,充分了解药物的不良反应及药物潜在的误用、滥用和成瘾风险。
7.3 对于高危患者可采取下述方法进行观察和监测
1)建议患者建立记录药物使用剂量和时间的“镇痛药物使用日记”。
2)医师对门诊患者“镇痛药物使用日记”中记录的信息进行核实。
3)阿片类药物使用前和治疗期间行尿检,可以监测不恰当的药物使用。
4)对于出现药物不恰当使用或存在高危因素的患者,可适当增加门诊就诊频率。
专家组成员
特邀顾问
王杰军 上海长征医院
秦叔逵 南京东部战区总医院
樊碧发 中日友好医院
刘延青 首都医科大学附属北京天坛医院
黄 诚 福建省肿瘤医院
学组组长
王 昆 天津医科大学肿瘤医院
编写秘书
邵月娟 天津医科大学肿瘤医院
组织成员(姓氏按拼音顺序)
白静慧 辽宁省肿瘤医院/中国医科大学肿瘤医院
陈冀衡 北京大学肿瘤医院
陈映霞 南京东部战区总医院
成文武 复旦大学附属肿瘤医院
冯智英 浙江大学医学院附属第一医院
金 毅 东部战区总医院
景年财 吉林省肿瘤医院
梁 锐 广西医科大学附属肿瘤医院
刘 波 山东省肿瘤医院
刘 芳 吉林大学第一医院
刘金锋 哈尔滨医科大学第二附属医院
刘 勇 东南大学医学院附属徐州医院/徐州市中心医院
路桂军 清华大学附属北京清华长庚医院
毛 勇 云南省肿瘤医院/昆明医科大学第三附属医院
宛春甫 河北医科大学第四医院
王 剑 中山大学肿瘤防治中心
王楠娅 吉林大学第一医院
王 琼 东南大学医学院附属江阴医院
王玉梅 中国医科大学附属盛京医院
维 拉 新疆医科大学附属肿瘤医院
吴敏慧 陕西省肿瘤医院
谢广伦 河南省肿瘤医院
熊源长 海军军医大学附属长海医院
杨金凤 湖南省肿瘤医院/中南大学湘雅医学院附属肿瘤医院
杨 扬 江苏省肿瘤医院
姚 明 嘉兴学院附属第一医院
张翠英 内蒙古自治区人民医院
周志国 湖南省肿瘤医院
邹慧超 哈尔滨医科大学附属肿瘤医院
参考文献
[1]van den Beuken-Van EM,de Rijke JM,Kessels AG,et al.Prevalence of pain in patients with cancer:a systematic review of the past 40 years[J].Ann Oncol,2007,18(9):1437-1449.
[2]Davies A,Buchanan A,Zeppetella G,et al.Breakthrough cancer pain:an observational study of 1000 European oncology patients[J].J Pain Symptom Manage,2013,46(5):619-628.
[3]Caraceni A,Martini C,Zecca E,et al.Breakthrough pain characteristics and syndromes in patients with cancer pain.An international survey[J].Palliat Med,2004,18(3):177-183.
[4]Portenoy RK,Hagen NA.Breakthrough pain:definition,prevalence and characteristics[J].Pain,1990,41(3):273-281.
[5]Fallon M,Giusti R,Aielli F,et al.Management of cancer pain in adult patients:ESMOClinical PracticeGuidelines[J].AnnOncol,2018,29(S4):v166-v191.
[6]Mercadante S,Marchetti P,Cuomo A,et al.Breakthrough pain and its treatment:critical review and recommendations of IOPS(Italian Oncologic Pain Survey)expert group[J].Supportive Care in Cancer,2016,24(2):961-968.
[7]Davies AN,Dickman A,Reid C,et al.The management of cancer-related breakthrough pain:recommendations of a task group of the science committee of the association for palliative medicine of great Britain and Ireland[J].Eur J Pain,2009,13(4):331-338.
[8]Zimmermann M,Richarz U.End-of-dose pain in chronic pain:does it vary with the use of different long-acting opioids[J]?Pain Pract,2014,14(8):757-769.
[9]Webber K,Davies AN,Zeppetella G,et al.Development and validation of the breakthrough pain assessment tool(BAT)in cancer patients[J].J Pain Symptom Manage,2014,48(4):619-631.
[10]Daeninck P,Gagnon B,Gallagher R,et al.Canadian recommendations for the management of breakthrough cancer pain[J].Current Oncol,2016,23(2):96-108.
[11]Esparza-Miñana JM.Diagnosis and treatment of breakthrough pain[J].Med Clin(Barc),2018,150(3):114-118.
[12]Mercadante S,Radbruch L,Caraceni A,et al.Episodic(breakthrough)pain:consensus conference of an expert working group of the European Association for Palliative Care[J].Cancer,2002,94(3):832-839.
[13]Wengstrom Y,Geerling J,Rustoen T.European oncology nursing society breakthrough cancer pain guidelines[J].Eur J Oncol Nurs,2014,18(2):127-131.
[14]NCCN.Adult cancer pain[J].NCCNClinPract GuideOncol,2013,(2):247-270.
[15]Corli O,Roberto A.Pharmacological and clinical differences among transmucosal fentanyl formulations for the treatment of breakthrough cancer pain:areviewarticle[J].MinervaAnestesiol,2014,80(10):1123-1134.
[16]Noble-Gresty J.Recent and upcoming approaches in the management of cancer breakthrough pain[J].Rev Pain,2010,4(2):2-7.
[17]Farrar JT,Cleary J,Rauck R,et al.Oral transmucosal fentanyl citrate:randomized,double-blinded,placebo-controlled trial for treatment of breakthrough pain in cancer patients[J].J Natl Cancer Inst,1998,90(8):611-616.
[18]Hagen NA,Fisher K,Victorino C,et al.A titration strategy is needed to manage breakthrough cancer pain effectively:observations from data pooled from three clinical trials[J].J Palliat Med,2007,10(1):47-55.
[19]Mercadante S,Marchetti P,Cuomo A,et al.Breakthrough pain and its treatment:critical review and recommendations of IOPS(Italian Oncologic Pain Survey)expert group[J].Support Care Cancer,2016,24(2):961-968.
[20]王昆,金毅.难治性癌痛专家共识(2017年版)[J].中国肿瘤临床,2017,44(16):787-793.
[21]Olarte JM.Breakthrough cancer pain and rational drug use[J].Support Care Cancer,2017,25(S1):11-17.
doi:10.3969/j.issn.1000-8179.2019.06.228
通信作者:王昆 wangk1128@sina.com