摘要
新中国成立后的不同时期,随着国内外麻醉药品和精神药品( 以下简称“麻精药品”) 种类和药物滥用情势的不断变化,我国麻精药品管制的政策和制度在传承中不断调整改革,进而跟进调整我国麻精药品管制品种目录,以适应当时药品监管形势和禁毒斗争形势的需要。以新中国麻精药品管制重要法律法规的颁布实施为研究基础,以麻精药品管制品种目录或麻精药品列管制度的重大变动为分期依据,可将1949 年新中国成立至 2019 年期间麻精药品管制品种目录的变动历程分为5个时期,依次分析各个时期目 录调整和变动的主要内容、特点、原因和意义等,为应对当前日益复杂的麻精药品管制问题和探讨改进我国 麻精药品列管制度提供回顾性研究视角。
关键词
麻醉药品; 精神药品; 毒品; 管制; 目录
正文
由于麻醉药品和精神药品( 以下简称“麻精药 品”) 特殊的医药理化性质,医疗目的连续使用或非医疗目的滥用均可致生理依赖性甚至精神依赖性,合法麻精药品流入非法渠道或者非法来源麻精药品 引发的毒品运输、贩卖、消费及衍生弊害等问题,可致严重的公共卫生问题和公共安全问题,这也是国家实施严格的麻精药品管制,开展严厉禁毒斗争的重要原因。我国对麻精药品实施国家管制最早可追溯至清朝雍正七年( 1729 年) 颁布的《惩办兴贩鸦片烟及开设烟馆条例》,此后对以鸦片为代表的“麻醉药品”类物质和随后的“精神药品”都实施了性质不 一、成效不一的国家管制。新中国成立后,政府高度重视麻精药品的管制工作,1950 年 11 月 1 日,由当时的原政务院核准原卫生部发布了《管理麻醉药品 暂行条例》和《供应麻醉药品暂行范围表》,这是新中国首次发布麻醉药品管理法规,并同时发布《麻 醉药品暂行范围表》,开启了新中国对麻醉药品及随后的限制性剧药( 新中国早期对精神药品的称 谓) 、精神药品、非药用类麻醉药品和精神药品等精神活性物质实施国家管制的历程。可以说,新中国麻精药品的管制工作是伴随着解决旧中国遗留下的鸦片问题开启的,并随着国内外麻精药品管制情势的日益复杂和毒品问题的不断变化逐步调整麻精药品管制种类,以适应当时药品监管形势和禁毒斗争形势的需要。麻精药品有效管制的前提是明确麻精药品管制的品种目录和种类范畴。我国现行麻精药品的管制品种目录是依照联合国药物管制公约的附表清单,并根据我国药品管理的相关法律法规等综合考虑制定发布的。麻精药品按特殊药品管理,列入目录的药品和其他物质还是《刑法》和《禁毒法》 授权认定为毒品品种的范畴。因此,清晰明确、科学合理、规范调整的麻精药品管制品种目录是开展特殊药品监管、医疗机构临床合理使用及禁毒部门开展毒品问题治理的前提和基础。当前,关于现行麻精药品监管制度及运行的研究成果较多,不乏从毒品角度分析毒品列管制度的研究成果,但从历史角度对麻精药品管制品种目录展开回顾性分析的研究成果较少。基于此,本文以法律文件、文献资料和历 史背景为研究依据,以 1949 年 10 月新中国成立至 2019 年 4 月我国对芬太尼类物质实施整类列管为研究时间范围,以麻精药品管制品种目录的变动历程为研究对象,依托我国麻精药品管制相关重要法 律法规的颁布实施为分期基础,以麻精药品管制品种目录或麻精药品列管制度的重大变动为分期依据,将中国麻精药品管制品种目录变动的历程 ( 1949—2019 年) 大致分为 5 个时期,并依次梳理分 析各个时期目录调整和变动的主要内容、特点、原因 和意义等,多视角分析中国麻精药品监管制度和管 制品种的变迁,这对于有效应对当前日益复杂的麻精药品管制问题和毒品治理问题,进一步探讨麻精 药品列管制度的改进方向等,均具有重要的理论意义、历史意义和现实意义。
1、 发布麻醉药品单一管制品种目录时期( 1949— 1963 年)
新中国成立之初,旧社会遗留的鸦片烟毒问题成为亟待大力整治的主要社会问题之一。1950 年 2 月,原政务院发布《关于严禁鸦片烟毒的通令》,掀 起了保护人民健康、恢复与发展生产、肃清鸦片烟毒 流行的大规模禁止烟毒运动,并取得了举世瞩目的 成效,产生了深刻的政治和社会影响。与此同时,合 法的“非传统意义上毒品”,即医药和研究科学上必需的麻醉药品管理问题受到国家重视并予以应对, 遂开始着手加强药品管制,特别是麻醉药品的管制工作。
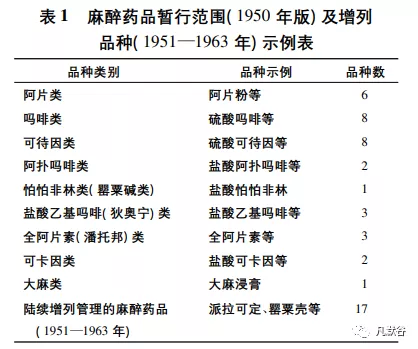
为供应医药及科研上必需的麻醉药品,防止不正当使用,充分发挥麻醉药品保障人民健康和福祉的医疗需要,1950 年 11 月 1 日原政务院核准原卫 生部发布《管理麻醉药品暂行条例》、《管理麻醉药 品暂行条例施行细则》和《供应麻醉药品暂行范围 表》,随后原政务院又核准原卫生部发布《麻醉药品 临时登记管理办法》,这些条例、细则、范围表和办 法等规范性文件的制定和发布是新中国麻精药品实施国家管制和发布品种目录的开端。《管理麻醉药品暂行条例》规定对阿片类、古柯( 高根) 类、大麻类 及其他经原卫生部指定有毒性、能成瘾癖的化学制 品等麻醉药品的输入、制造、供应、购用及稽核依照 本条例管理[1]。在首份《供应麻醉药品暂行范围 表》中共有 9 大类 34 种麻醉药品纳入管制[1],见表 1。虽然我国社会长期以来深受鸦片烟毒危害而对 鸦片形成了高度负面印象,但鸦片类物质的医药价 值及科研的需求应给予保障。《管理麻醉药品暂行 条例施行细则》第 5 条和第 6 条规定: 麻醉药品的详细名称暂以《供应麻醉药品暂行范围表》所载者为标准,若有科学机关和团体提出正式报告,经原中央卫生研究机关审查,认为可供医药科学试验研究应用者,由原卫生部呈请原政务院特许[1]。这些条款可以视作当时麻醉药品列管的实体和程序标准的初 步规定。据单一资料源显示[1],1951—1963 年,原 卫生部又陆续发布了应予管理的麻醉药品种类的通 知达 13 次,不断增列需要管制的麻醉药品累计达 17 种,这一时期共将 51 种麻醉药品纳入管制范围。这一系列举措显示在新中国成立初期麻醉药品的增 列或变动已呈现动态调整的特征,主要是通过原卫 生部发布通知、回复批复等形式,及时将需按麻醉药 品管制的药品纳入管制。
值得注意的是,此时期尚无精神药品称谓和概念,国家层面也没有发布规范性的法律文件管制具有现今意义上的精神药品类的物质。但此类物质同 样存在滥用的问题。例如,1952 年重庆市发生去氧 麻黄碱( 同去氧麻黄素、甲基苯丙胺) 成瘾问题,原 卫生部首次发布关于去氧麻黄碱应按剧药范围管理 的通知[1]。随着类似滥用事件的发生,多个部门先后发布了相关文件管理此类药品,逐步加强对去氧 麻黄碱的管制力度。对现今意义上的精神药品以剧 药等为名称进行探索性管制的做法,为下一步制定 规范性的法律文件依法管制精神药品类物质奠定了基础,所以此时期称为发布麻醉药品单一管制品种 目录发布时期。综上可知,新中国成立初期的麻醉 药品管理逐渐进入有法可依的阶段,一系列法律条 款防止了合法渠道的麻醉药品流入非法渠道,没有造成严重的流弊和产生不良社会影响,进而对鸦片 烟毒形成全方位管制,为正在进行的禁止鸦片烟毒 运动的顺利开展并取得最终胜利发挥了重要促进作用[2]。
2、以麻醉药品和限制性剧药称谓发布品种目录时期( 1964—1984 年)
新中国成立初期,原卫生部将现今意义上的一 些精神药品或类似精神药品物质曾分别以“剧药”、 “毒剧药品”、“限制性剧药”等称谓进行管理[3],这 些名称的内涵在当时也是有差异的,称谓的频繁变 动和混合使用表明当时对此类药品药理性质和药品 管理定位认识不断深化。例如,1963 年原卫生部党组在《关于加强去氧麻黄素等毒剧药品管理的报 告》中以毒剧药品指代在一些地区出现滥用的去氧麻黄素等物质[4]。由于此时期我国药品行业并未真正形成一个独立的产业,化学制药业、药品商业流 通分别作为化工和商业领域的组成,使得药品监管 的职能设置呈现多部门共管的局面,药政管理的法 律文件也多由多部门共同发布[5]。1963 年 10 月, 原卫生部会同原化学工业部、原商业部共同发布 《关于药政管理的若干规定( 草案) 》,这是新中国成 立后有关药政管理的第一个综合性法规文件,该规定设置专章对麻醉药品、毒药和限制性剧药的管理 进行规范,该药品法规由多部门联合发布。1964 年 4 月,原卫生部联合化工部、商业部,根据《关于药政 管理的若干规定( 草案) 》第 46 条 ~ 第 49 条的规 定,出于“为了保证防止疾病的需要,正确使用毒 药、限剧药,防止乱产、乱销和乱用,保障人民健康” 的目的,正式制定发布了《管理毒药、限制性剧药暂 行规定》,并以附件形式发布《西药毒药、限制性剧 药品种及分类表》,这是我国首个国家层面关于限制性剧药管理的规范性法律文件和品种及分类表。该规定除了明确毒药、限剧药的品种范畴和管理办法外,对增列品种的途径也做了规定,即“各省、自治区、直辖市卫生厅、局可结合当时、当地具体情况, 研究增订品种,报原卫生部审批”,为了便于管理, 该规定暂将毒药、限制性剧药分为 3 类进行管理,不同类别药品的生产、供应、购买和使用具有不同的管理规定。《西药毒药、限制性剧药品种及分类表》中 将西药毒药和限剧药混列在一起分类列示,其中限 制性剧药第一类 3 种、第二类 1 种、第三类 14 种,这 可看作是新中国最早的精神药品品种目录,也是对 精神药品实施分类管理的最早雏形,见表 2 [1]。需 要说明的是,这一分类表虽将西药毒药与限剧药混 在一起,但对每一品种的归属和例外情况都做了明 确标注。例如,当时认为麻醉药品是指能成瘾癖的 毒性药品,此规定不包括属于麻醉药品的毒、限剧药及中药毒性药品,但附表第二类的“复方樟脑酊、含 阿片的复方甘草片和复方甘草合剂”虽含麻醉药 品,但不属于限剧药范围,因容易发生流弊,一并列 入附表加强管理。这些分类设置和名称称谓看上去 略显混乱,一方面反映了当时对毒药( 又分中药毒 药和西药毒药) 、剧药、限剧药、麻醉药品认识上的 模糊,另一方面也可看出当时对此类物质开展分类 列管的积极探索。

1978 年 7 月,国务院批准颁布了原卫生部制定的《药政管理条例( 试行) 》,这是新中国成立后药政管理领域的第 2 个系统管理法规,该法规成为后来 原卫生部牵头起草《药政法( 草案) 》( 《药品管理 法》的前身) 的基础。根据《药政管理条例( 试行) 》 的第 39 条、第 40 条的规定,原卫生部出于“为防病 治病的需要,防止流弊”的目的,于 1979 年 6 月发布 《关于医疗用毒药、限制性剧药管理规定》。该规定将毒药、限剧药分为 2 类,以《西药毒药、限剧药品 种及分类表》的形式分类列示,其中第一类毒药和限剧药共 14 种,第二类毒药和限剧药共 17 种,见表 3。与 1964 年版的“西药毒药、限制性剧药品种及分 类表”不同的是,该分类表将“西药毒药”、“限剧药” 由 1964 年版的三大类调整为两大类,且没有标明各品种是西药毒药还是限剧药,也没有明确说明分类 的依据。但整体上第一类比第二类在供应范围、零 售范围和保管措施等方面均较严格,且很多品种的 归类相较于 1964 年版出现调整。该规定第 17 条 “附表未包括的毒、限剧药,如有必要管理,各省、市、自治区卫生局、医药管理局,可结合当地情况增 订,并报原卫生部及原国家医药管理总局备案。”可 视为是“增列品种”的规定,这一规定虽对增列品种 的情形表述模糊,但也指明了增列品种的主体部门、 部门层级以及报批程序。

在麻醉药品管制方面,国务院根据当时麻醉药品管制形势和需要,于 1978 年 9 月重新修订并发布施行新的《麻醉药品管理条例》,重新加强麻醉药品的管理。该条例将麻醉药品界定为能成瘾 癖的毒性药品,并进一步指出“使用得当,可以治病,使用不当,就会发生流弊,危害人民”,麻醉药品的管理范围包括阿片类、吗啡类、可卡因类及原卫生部指定的其他易成瘾癖的毒性药品。这些关于麻醉药品内涵和范围的界定,从某种意义上讲是 兼具科学判断和朴素认知的综合概括。根据1978 年 9 月发布的《麻醉药品管理条例》所附《麻醉药品 品种范围表》,将麻醉药品分为 12 大类,共 39 种,见 表 4。

此次麻醉药品品种范围表是继 1950 年首版《供 应麻醉药品暂行范围表》后的第 2 版麻醉药品管制 品种范围表,并于 1979 年 2 月发布《每季购用限量表》。此条例明确了麻醉药品属于计划供应范畴, 进一步强化政府主管部门管制,但客观上对医疗机 构的使用带来不便,严格管制和合理使用之间的矛盾逐渐呈现。
3、 以麻精药品称谓发布品种目录时期( 1985—2004 年)
1985 年实施的《药品管理法》第一次以法律文 本的形式对药品的研制、生产、经营和使用作出规定,标志着我国药品监管开始进入法制化轨道[6]。1964—1984 年,我国法律文件中一般将精神药品笼 统称为毒药、限制性剧药,而《药品管理法》为了在称谓上与国际药物管制公约接轨,将这类药品正式更名为精神药品,属于特殊管理的药品。《药品管 理法》的颁布为系统地建立我国麻精药品管制相关法律法规提供了上位法依据。与此同时,为积极参 与国际药物管制合作,履行国际禁毒义务,1985 年我国同时决定加入联合国《经1972 年议定书修正的 1961 年麻醉品单一公约》和《1971 年精神药物公 约》,正式融入全球药物管制体系,积极响应麻精药 品的国际管制义务。随 后,依 照 国 内《药 品 管 理 法》的规定和国际药物管制公约对缔约国的一般 义务要求,在总结了我国麻精药品管理经验的基 础上,国务院分别于 1987 年 11 月和 1988 年 12 月 颁布施行了《麻醉药品管理办法》和《精神药品管 理办法》,对我国麻精药品的管理作了全新的系统规定。
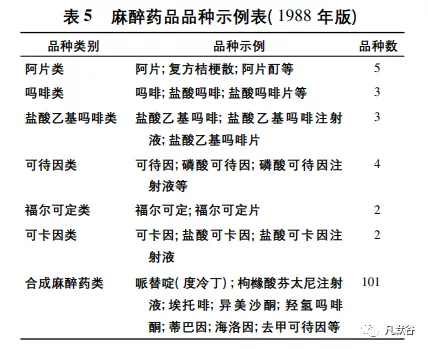
在《麻醉药品管理办法》颁布施行前,在原卫生部发布的《关于罂粟碱、阿扑吗啡和烯炳吗啡不再列入麻醉药品管理范围的通知》中指出,基于“临床 使用中均未发现有产生药物依赖性的作用,国内外 医学文献未见有产生药物依赖性的报道,征求各方 面临床医学专家的意见”3 个方面的考虑做出关于 这 3 种药品不再列入麻醉药品管理范围的决定[7]。在之前讨论的卫生主管部门等授权部门发布的规范性文件中曾多次出现增订品种的实体或程序条款, 但从未出现过“退出或移除”的条款规定。这一通知的发布意味着我国事实上已经建立了管制药物的退出和增订的动态调整机制。这一动态调整机制其 实是符合国际药物管制公约的精神,不排除是借鉴 或根据国际药物管制公约的相关条款的精神做出的 上述调整。但新办法的条文中没有明确指出麻醉药 品增列调整的途径,通过列举加概括的方式指出麻醉药品包括阿片类、可卡因类、大麻类、合成麻醉药 类及原卫生部指定的其他易成瘾癖的药品、药用原植物及其制剂,这一界定为原卫生部后续发布新版品种表提供了依据。1988 年 2 月,原卫生部根据 《麻醉药品管理办法》第 3 条、联合国《1961 年麻 醉品单一公约》及我国麻醉药品使用情况,发布新 版《麻醉药品品种表》通知[8],共分七大类,120 种 麻醉药品,主要是大幅增加了合成麻醉药类品种, 见表 5。
在《精神药品管理办法》颁布施行前,1986 年 6 月,原卫生部、原国家医药管理局发布《关于将强 痛定列入精神药品管理的通知》,这是我国 1985 年实施《药品管理法》和 1985 年加入《1971 年精神药物公约》后,第一个按精神药品管理的药品。根据《精神药品管理办法》规定,精神药品是指直接作用于中枢神经系统,使之兴奋或抑制,连续使用能产生依赖性的药品。并依据精神药品使人体产生的依赖性和危害人体健康的程度,分为第一类和第二 类,各类精神药品品种由原卫生部确定。1989 年 2 月,原卫生部根据《精神药品管理办法》、 我国精神药品临床使用情况和联合国《1971 年精神 药品公约》公布的精神药品品种及分类,第一次以 精神药品称谓发布《精神药品品种及分类表》[9],该分类表采用了类似 1979 年版限制性剧药的分类 方法,将精神药品分为第一类和第二类分别管理, 其中第一类精神药品 39 种,第二类精神药品 65 种,见表 6。

上述麻精药品品种目录的发布基本奠定了现今 我国麻精药品品种目录设置和分类的基础,后续麻精药品品种目录的不断变动是在此版目录基础上的增加、减少、调整及创新,并随国际管制药物公约目 录的变动调整。例如,1996 年 1 月,原卫生部发布更新《麻醉药品品种目录》( 118 种) 和《精神药品品 种目录》( 第一类精神药品 47 种、第二类精神药品 72 种) 。这次调整的背景也是根据《1971 年精神药 物公约》所附清单品种种类变动而大幅度增加了精 神药品管制品种的种类,因为国际药物管制公约规定缔约国应最低限度将公约附表所列物质纳入本国管制品种目录。例如,2001 年 5 月,原国家药品监督管理局发布《关于将唑吡坦等 4 种药物纳入精神 药品管理的通知》[10],该通知直接点明本次增列就 是根据联合国麻醉药品委员会的决议而做出的相应 调整。纵览 20 世纪 80 年代中期至 21 世纪初,自我国加入国际药物管制公约后,我国麻精药品的管制制度和品种目录逐步与国际接轨,并呈现出法制化 和国际化的特征。
4 统一发布麻醉药品和精神药品品种目录时期 ( 2005—2014 年)
2005 年 8 月,国务院发布《麻醉药品和精神药 品管理条例》后,2005 年 11 月,原国家食品药品监 督管理局、公安部、原卫生部联合发布2005 年版“麻醉药品和精神药品品种目录”,其中麻醉药品 121 种,第一类精神药品 52 种,第二类精神药品 78 种, 共计 251 种。自此,我国麻醉药品和精神药品进入统一管理、统一发布麻醉药品和精神药品品种目录时期。此次条例和目录的调整主要是根据上位法 《药品管理法》的修订和国务院药监机构改革而做 出的调整,此外也包括国际药物公约管制目录的变动和国内药物滥用的新形势做出的调整。若从麻精药品管制品种种类的角度审视该条例,呈现出以下新变化: ① 进一步明确了我国麻精药品管制的目的,相较以往更加强调麻精药品的“合法、安全、合理使用”。② 对麻精药品的概念做出较大调整,即 “是指列入麻醉药品目录、精神药品目录的药品和其他物质”。这一表述是以“列举目录”的方式界定麻精药品的概念,并且说明麻精药品不仅包括列入 麻精药品目录中的“药品”,还包括“其他物质”,这 一表述为拓展麻醉药品和精神药品的管制种类范围预留了解释空间。③ 明确指出麻精药品的目录由国务院药品监督管理部门会同国务院公安部门、国 务院卫生主管部门制定、调整并公布。这是我国首 次明确国务院药品监督管理部门为麻精药品目录制定、调整和发布的主体部门,首次明确国务院公安部门是麻精药品目录制定、调整和发布的参与部门。④ 对增列新品种和调整精神药品分类的标准和程 序也作出了基本规定,标准为“发生滥用”、“已经造成或者可能造成严重社会危害的”,程序是“国 务院药品监督管理部门会同国务院公安部门、国 务院卫生主管部门应当及时将该药品和该物质列 入目录或者将该第二类精神药品调整为第一类精 神药品”。这些规定标志着我国麻精药品目录的制定、调整和发布等变动机制已进入规范化、法制 化阶段。其后,国务院药品监督管理部门会同国务院公安部门和卫生主管部门分别于 2007 年 10 月和 2013 年 11 月 2 次统一发布《麻醉药品和精 神药品品种目录》,继续保持麻醉药品和第一类、 第二类精神药品统一、分类管理的制度,麻精药品管制品种的数量均发生一定变动,总体变动情况见表 7。

5 非药用类麻精药品管制品种增补目录开始发布 时期( 2015—2019 年
2015 年 9 月,公安部、原国家卫生和计划生育 委员会、原国家食品药品监督管理总局、国家禁毒委员会办公室联合发布《非药用类麻醉药品和精神药 品列管办法》,并同步发布《非药用类麻醉药品和精 神药品管制品种增补目录》。该办法所称的非药用 类麻醉药品和精神药品是指未作为药品生产和使 用,具有成瘾性或成瘾潜力且易被滥用的物质。这 是我国首次使用“非药用类麻醉药品和精神药品” 的表述,增补的非药用类麻精药品管制品种以附表 列示,一次性列管共计 116 种[11]。该办法首次规定 我国“麻醉药品和精神药品按照药用类和非药用类 分类列管”,并详细规定了新增非药用类麻精药品 管制品种的列管办法,包括列管目的、非药用类麻精药品的界定、非药用类麻精药品的列管主体、非药用类麻精药品调整至药用类的麻精药品目录的条件、 增列非药用类的麻精药品的程序和步骤等。非药用类麻精药品列管办法和增补管制品种目录主要是应对国内外日益突出的新精神活性物质( new psychoactive substances,NPS) 问题而设计发布的。其实,早在 2001 年我国已将氯胺酮列入第二类精神药品 管制[12],这是我国最早开始管制的新精神活性物 质。自 2010 年以来,四甲基甲卡西酮等 13 种新精 神活性物质已先后列入《麻醉药品和精神药品目录》中[13]。2015 年《非药用类麻醉药品和精神药品 列管办法》颁布实施后,该办法已成为我国常态化增 列新精神活性物质的重要依据。2017—2018 年,我 国先后 3 次发布公告增列 40 种新精神活性物质列 入《非药用类麻精药品管制品种增补目录》[14 - 16]; 2019 年 4 月,公安部、国家卫生健康委员会和国家 药品监督管理局发布公告将芬太尼类物质列入非药用类麻醉药品和精神药品管制品种增补目录[17]。这是我国首次对某单一类物质实行整类列管,这意味着此后可能出现的所有芬太尼类物质在我国均被 视为非药用类麻醉药品和精神药品而受到严格管制,这标志着我国“芬太尼类物质”整类列管制度的正式建立,这是我国麻醉药品和精神药品列管制度的重大创新,也是中国禁毒法制建设历程中的重要 事件。至此,我国已累计列管的新精神活性物质达 “170 + n”种,因芬太尼类物质衍生物质种类不确 定,笔者将该类物质管制品种数暂定为 n 进行计数, 且为≥0 的整数,见表 8。

非药用类麻醉药品和精神药品目录中列管的品种大多是没有或暂时没有发现医药价值的一类具有成瘾性或者成瘾潜力且易被滥用的物质,同样可引发严重的公共卫生问题和公共安全问题。但国内外对新精神活性物质的关注更多出于公共安全问题的忧虑,而非物质本身所蕴含的医药价值,这是此类物 质与以往纳入监管的麻精药品的关注点的最大不同。新精神活性物质具有制造上的主观故意性、合理用途的不确定性、法律上的非全管制性、种类上的多样性和快速更新性、滥用人群的广泛性以及社会危害的严重性等特点[18]。新精神活性物质出现的最主要原因是规避现行管制制度的法律制裁,它的出现对传统的毒品管制制度或麻精药品管制制度提出了挑战。新精神活性物质的产生与泛滥,并非毒 品品项或功能的自然进化,而是毒品列管制度的缺陷与难以根除的毒品消费需求之间固有矛盾的衍生现象[19]。全球毒品在滥用种类、滥用结构、制造贩运方面不断发生新的变化,如何强化新精神活性物质的管制,及时增列至管制品种目录,防止其非法生产、经营、运输、使用和进出口是国内外禁毒执法部门和药物滥用防治研究者关注的焦点和热点问题。因此,《非药用类麻醉药品和精神药品列管办法》的 颁布实施,在我国麻精药品管制制度和毒品列管制度上具有重大理论意义和现实意义。该办法的出台 受到国内外的高度关注,对我国麻精药品管制制度的完善,增进国际药物管制执法合作,打击毒品违法 犯罪活动提供了制度基础和法律依据。
结语
麻精药品兼具特殊的医药理化性质、丰富的文化社会内涵、沉重的历史负担和现实压力等特征,历来是各国政府管制的重点。截至 2020年1月1日,中国现行列管的药用类和非药用类麻醉药品和精神药品的品种种类累计已达431 + n 种,其中,麻醉药品121种、精神药品154 种(第一类精神药品 69 种, 第二类精神药品 85 种) 、非药用类麻精药品 156 + n 种,分别归类至《麻醉药品品种目录》2013 年版、《精神药品品种目录》2013 年版、《非药用类麻醉药品和 精神药品管制品种增补目录》2015 年版,以及陆续 以公告的形式增列于上述目录中的品种。
本文通过系统梳理分析1949年新中国成立至2019年麻精药品管制品种目录变动的脉络,并以此视角观察中国麻精药品管制乃至毒品问题治理的理念和思路。通过新中国70年麻精药品管制品种目录变动的历程可知,这种变动和调整是常态的、动态的和多样的,主要包括目录的增设、列管的方式、品种的调整等,既有管制品种的增列和转移,也有管制品种的减列和更名,更有列管标准和程序的创新和丰富等。这些丰富的麻精药品管制实践为解决现今麻精药品管制难题和改进麻精药品列管制度提供了丰富的历史视角和经验参考。一个清晰明确、科学规范、符合实际、具有可预期的动态调整机制应是未来我国麻精药品管制品种目录发展的方向。纵览新中国70年麻精药品管制品种目录变动的历程还可发现,我国麻精药品管制品种目录的调整和变动深 受历史背景、政治因素、国际环境、科技水平、滥用形势等的综合影响,从麻精药品的称谓名称、内涵界定、管制目的、种类范围、增列减列以及发布主体、列 管标准、列管程序、变动时间、调整频次等诸多方面, 在传承和调整中不断优化、改进、创新列管制度,保障我国麻精药品在医疗、教学、科研、工业等方面的合理、合法和安全使用,这对有效预防和打击麻精药品流入非法渠道引发的毒品违法犯罪行为,推动麻精药品在保障合理使用与严格管制之间取得 平衡,适应药品监管形势和禁毒斗争形势的需要意义重大。
当前,我国麻精药品监管和毒品问题治理的形势依然严峻复杂,面对不断出现的新形势、新问题、 新挑战,从新中国成立70年来麻精药品管制品种目 录变动的脉络中发现可借鉴的经验和做法,为构建和创新符合我国实际的麻精药品列管制度提供史学 视角和决策参考,为进一步探究国际麻精药品管制目录变动问题提供研究基础,为深度参与国际药物 管制事务贡献中国智慧。
参考文献
[1] 北京市卫生局编印,药政管理文件汇编( 第一辑) [M]. 1965.
[2] 王金香.中国禁毒史[M].上海: 上海人民出版社,2005: 296 -298.
[3] 周邦元.談毒剧药的管理[J]. 中国药学杂志,1957,5 ( 1) :15 - 17.
[4] 中央批转卫生部党组关于加强去氧麻黄素等毒剧药品管理的报告( 中发[63]132 号)[S].1963.
[5] 陆悦.壮丽 70 年·中国药监记忆法律法规篇: 在依法治药轨道上阔步前行[N]. 中国医药报,2019 - 09 - 27.
[6] 刘子晨. 医药工业 70 年变迁: 腾云巨变[EB/OL]. ( 2019 - 10 -07) .“E 药经理人”微信公众号.
[7] 卫生部. 关于罂粟碱、阿扑吗啡和烯炳吗啡不再列入麻醉药品管理范围的通知[S]. 1987.
[8] 卫生部. 关于贯彻执行《麻醉药品管理办法》的通知[S].1988.
[9] 海关总署. 关于转发“精神药品品种及分类”的通知[S].1989.
[10] 国家药品监督管理局. 关于将唑吡坦等 4 种药物纳入精神药品管理的通知[S ] 2001.
[11] 公安部,国家卫生和计划生育委员会,国家食品药品监督管理总局,国家禁毒委员会 办公室. 关于印发《非药用类麻醉药品和精神药品列管办法》的通知[S]. 2015.
[12] 国家药品监督管理局. 关于氯胺酮管理问题的通知[S].2001.
[13] 新华网. 国家禁毒办: 又有 32 种新精神活性物质列入管制![EB/OL].[2018 - 08 - 29]. http: / /www. xinhuanet. com/legal / 2018 - 08 /29 /c_129942388. htm.
[14] 公安部,国家食品药品监督管理总局,国家卫生和计划生育委员会. 关于将卡芬太尼等四种芬太尼类物质列入非药用类麻醉药品和精神药品管制品种增补目录的公告 [S]. 2017.
[15] 公安部,国家食品药品监督管理总局,国家卫生和计划生育委员会. 关于将 N-甲基- N-( 2-二甲氨基环己基) -3,4-二氯苯甲酰胺( U-47700) 等四种物质列入非药用类麻醉药品和精神药品管制品种增补目录的公告[S]. 2017.
[16] 公安部,国家卫生健康委员会,国家药品监督管理局. 关于将4-氯乙卡西酮等 32 种物质列入非药用类麻醉药品和精神药品管制品种增补目录的公告[S]. 2018.
[17] 公安部,国家卫生健康委员会,国家药品监督管理局. 关于将芬太尼类物质列入《非药用类麻醉药品和精神药品管制品种增补目录》的公告[S]. 2019.
[18] 肖扬. 新精神活性物质蔓延成国际禁毒一大难题[J]. 上海化工,2017,42( 3) : 52 - 53.
[19] 包涵. 新精神活性物质管制的国际经验和中国路径[J]. 公安学研究,2018,1( 3) : 44 - 63,123.
作者:陈帅锋,甄 橙,史录文
作者单位:北京大学医学人文学院,中国人民公安大学侦查学院,北京大学药学院
论文题目:中国麻醉药品和精神药品管制品种目录变动历程研究( 1949—2019 年)
发表期刊:《中国新药杂志》2021年第30卷第11期
---本文经论文作者及通讯作者同意后发布---